Ce sunt radiatiile?
Radiaţii ionizante şi radiaţii neionizante
Din punct de vedere al protecţiei împotriva radiaţiei, radiaţiile se împart în 2 categorii: ne-ionizante şi ionizante, pentru a sublinia pericolul la adresa sănătăţii oamenilor. Radiaţiile electromagnetice: lumina, radiaţiile ultraviolete şi infraroşii, undele radio, microundele, ultrasunetele aparţin primei categorii.
Când radiaţiile lovesc un atom, îşi transferă o parte din energie asupra acestuia. Dacă energia transferată de radiaţie este suficient de mare, se produce ionizarea - procesul de îndepărtare a unui electron din atom, care lasă în urmă 2 particule încărcate electric – un electron şi un ion pozitiv. Prezenţa în număr mare a unor astfel de particule încărcate electric pot crea distrugeri ţesuturilor vii. Radiaţiile care pot transfera suficientă energie pentru a face acest lucru se numesc radiaţii ionizante, iar cele cu un nivel de energie mai scăzut sunt cele neionizante. Deşi anumite tipuri de radiaţii neionizante pot fi dăunătoare în doze mari, radiaţiile ionizante sunt, de regulă, mult mai periculoase. Atunci când oamenii vorbesc despre radiaţii, de regulă se referă la radiaţii ionizante.
Materia este formată din atomi, care se combină pentru a forma molecule. Un atom este format dintr-un nucleu cu dimensiuni foarte mici dar cu greutate relativ mare, înconjurat de electroni foarte uşori. Nucleul conţine un anumit număr de protoni, fiecare dintre aceştia cu sarcină pozitivă, iar numărul electronilor cu sarcină negativă este egal cu numărul protonilor, astfel încât atomul este neutru.
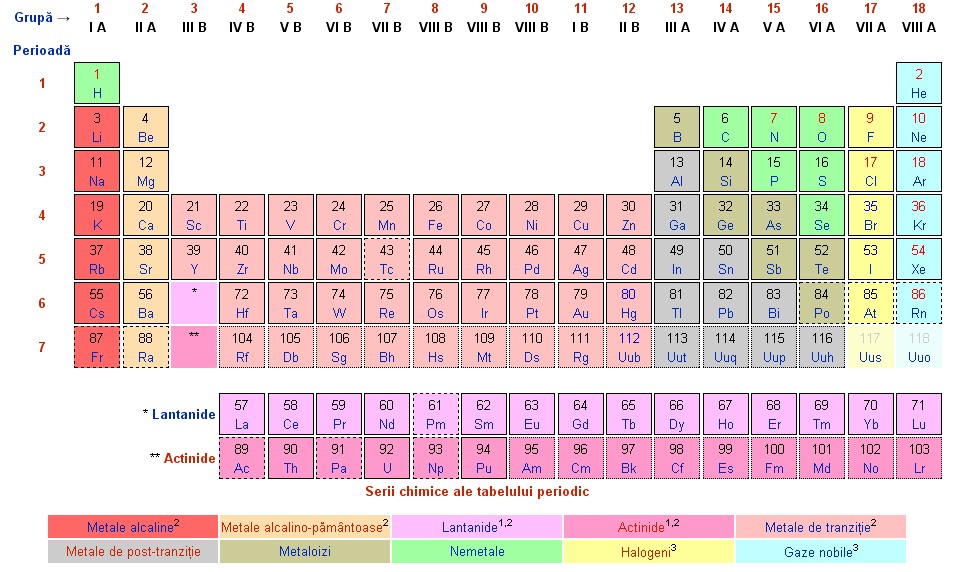
Fiecare atom este caracterizat de 2 numere: Z, numărul atomic care este dat de numărul protonilor (=numărul electronilor) şi A, masa atomică, care reprezintă numărul total de protoni şi neutroni din nucleu. Z identifică elementul chimic căruia îi aparţine atomul – oxigen, carbon, fier şi proprietăţile acestuia (de exemplu, oxigenul este gaz, fierul este metal, etc). În natură există 92 de elemente – de la hidrogen (Z = 1) la uraniu (Z=92) şi mai există un număr de aproximativ 20 de elemente (cu Z de le 93 la peste 110) care au fost obţinute artificial.
Fiecare atom este caracterizat de 2 numere: Z, numărul atomic care este dat de numărul protonilor (=numărul electronilor) şi A, masa atomică, care reprezintă numărul total de protoni şi neutroni din nucleu. Z identifică elementul chimic căruia îi aparţine atomul – oxigen, carbon, fier şi proprietăţile acestuia (de exemplu, oxigenul este gaz, fierul este metal, etc). În natură există 92 de elemente – de la hidrogen (Z = 1) la uraniu (Z=92) şi mai există un număr de aproximativ 20 de elemente (cu Z de le 93 la peste 110) care au fost obţinute artificial.
Atomul este cea mai mică particulă care păstrează proprietăţile fizice şi chimice ale unui element chimic.
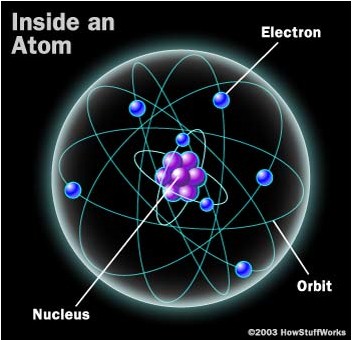 Fig. 1 – prezentarea clasica a atomului, folosind Modelul Rutherford-Bohr care reprezintă atomul ca cavând nucleul, încărcat pozitiv, compus din protoni (particule pozitive) şi neutroni (particule neutre), înconjurat de sarcini negative, elctronii. Numărul electronilor este egal cu cel al protonilor, deci atomul este neutru din punct de vedre electric.
Fig. 1 – prezentarea clasica a atomului, folosind Modelul Rutherford-Bohr care reprezintă atomul ca cavând nucleul, încărcat pozitiv, compus din protoni (particule pozitive) şi neutroni (particule neutre), înconjurat de sarcini negative, elctronii. Numărul electronilor este egal cu cel al protonilor, deci atomul este neutru din punct de vedre electric.
 Fig. 2 - prezentare a structurii atomice pentru atomul de heliu. Partea întunecată a norului electronic corespunde probabilităţii maxime de existenţă a electronului orbital 1s. Structura mărită a nucleului este prezentată schematic, cu roz sunt indicaţi protonii, iar cu albastru neutronii. În realitate, nucleul (şi funcţiile de undă ale fiecărui nucleon) este simetric din punct de vedere sferic (cazul nucleilor mai complexi).
Fig. 2 - prezentare a structurii atomice pentru atomul de heliu. Partea întunecată a norului electronic corespunde probabilităţii maxime de existenţă a electronului orbital 1s. Structura mărită a nucleului este prezentată schematic, cu roz sunt indicaţi protonii, iar cu albastru neutronii. În realitate, nucleul (şi funcţiile de undă ale fiecărui nucleon) este simetric din punct de vedere sferic (cazul nucleilor mai complexi).
 Fig. 3 - Înainte de 1961, se acceptau ca particule subatomice doar electronii, protonii şi neutronii. Azi se cunoaşte că protonii şi neutronii înşişi sunt constituiţi din particule şi mai mici numite quarci. În plus, electronul are un partener neutru din punct de vedere electric, aproape fără masă, numit neutrino. Electronul şi neutrino sunt ambii leptoni. Prin urmare, atomii sunt compuşi numai din quarci şi leptoni. Protonul (roz) este format din doi quarci "up" (roşu) şi un quarc "down" (albastru), iar neutronul (gri) este format din doi quarci "down" şi un quarc "up". Deşi nu apar în substanţa obişnuită, alte două generaţii mai grele de quarci şi leptoni pot fi generate în ciocnirile de înaltă energie. O importanţă deosebită pentru atom o prezintă bozonii, adică particulele de transport al forţelor de interacţiune. Astfel, electronii sunt legaţi de nucleu prin intermediul fotonilor ce transportă forţa electromagnetică. Protonii şi neutronii sunt menţinuţi împreună în nucleu prin intermediul gluonilor (negru) ce transportă forţa nucleară.
Fig. 3 - Înainte de 1961, se acceptau ca particule subatomice doar electronii, protonii şi neutronii. Azi se cunoaşte că protonii şi neutronii înşişi sunt constituiţi din particule şi mai mici numite quarci. În plus, electronul are un partener neutru din punct de vedere electric, aproape fără masă, numit neutrino. Electronul şi neutrino sunt ambii leptoni. Prin urmare, atomii sunt compuşi numai din quarci şi leptoni. Protonul (roz) este format din doi quarci "up" (roşu) şi un quarc "down" (albastru), iar neutronul (gri) este format din doi quarci "down" şi un quarc "up". Deşi nu apar în substanţa obişnuită, alte două generaţii mai grele de quarci şi leptoni pot fi generate în ciocnirile de înaltă energie. O importanţă deosebită pentru atom o prezintă bozonii, adică particulele de transport al forţelor de interacţiune. Astfel, electronii sunt legaţi de nucleu prin intermediul fotonilor ce transportă forţa electromagnetică. Protonii şi neutronii sunt menţinuţi împreună în nucleu prin intermediul gluonilor (negru) ce transportă forţa nucleară.Nucleele care conţin acelaşi număr de protoni (şi, prin urmare, sunt acelaşi element), dar numere diferite de neutroni (deci au numere atomice diferite) se numesc izotopi. De exemplu, U-234 (92 protoni, 142 neutroni), U-235 (143 neutroni) şi U-238 (146 neutroni) sunt cu toţii izotopi de uraniu. Orice nucleu atomic, având un Z şi un A se cheamă nuclid. Fiecare nuclid este deci caracterizat de numele elementului şi de masa sa atomică; de exemplu, azot-14 (N-14) sau stronţiu-90 (Sr-90). În limbajul curent, termenii de nuclid şi izotop sunt folosiţi deseori pentru acelaşi lucru.
Dezintegrarea radioactivă
Radioactivitatea este capacitatea dezintegrării spontane a unui atom. În acest fel se formează un nou atom prin eliberea unei radiaţii. Un atom poate emite trei tipuri de radiaţie radioactivă: radiaţia alfa pozitivă, radiaţia beta negativă şi radiaţia gama neutră din punct de vedere electric.
În timpul dezintegrării radioactive un element nu emite toate tipurile de radiaţii în acelaşi timp.
În timpul dezintegrării radioactive un element nu emite toate tipurile de radiaţii în acelaşi timp.
Majoritatea nuclizilor din natură sunt stabili, dar există anumiţi nuclizi existenţi în natură sau produşi de om – care au proprietatea numită radioactivitate. Aceştia se numesc radionuclizi.
Dezintegrarea este un proces aleatoriu – nu poate fi prevăzut momentul în care un anume nucleu se va dezintegra – dar ritmul mediu de dezintegrare al nucleului şi tipul de radiaţie pe care o emite sunt caracteristici ale radionuclidului.
 |
 |
| Semnul consacrat pentru radiaţii. | Simbolul suplimentar care indică radiaţiile, anunţat de AIEA în 2007. |
Unităţi de măsură pentru radioactivitate
Ritmul în care un radionuclid se dezintegrează se numeşte activitate – numărul mediu de dezintegrări pe secundă. Activitatea unei probe este numărul de atomi din probă înmulţit cu factorul λ (litera grecească lambda), care este o caracteristică constantă a radionuclidului.
Unitatea de activitate este dezintegrare pe secundă şi are un nume special, becquerel (Bq). 1 Bq este o dezintegrare pe secundă.1 Bq este un nivel foarte redus de activitate, aşa că, adesea, valorile sunt exprimate în kBq (mii de Bq) sau MBq (milioane de Bq) şi chiar GBq (miliarde de Bq).
Unitatea de activitate tolerată este 1 Ci (Curie) = 3,7 x 1010 dez/s = 3,7 x 1010 Bq.
O unitate de măsură înrudită pentru ritmul cu care un radionuclid se dezintegrează este timpul de înjumătăţire fizică (T1/2 sau Tf), de asemenea o caracteristică constantă a radionuclidului. Acesta reprezintă intervalul mediu necesar pentru ca o jumătate din atomii dintr-o probă de radionuclid să se dezintegreze.
Tipuri de radiaţii ionizante şi puterea lor de penetrare
Diferite surse emit diferite tipuri de radiaţii ionizante:
- Radiaţia alfa (α), de fapt atomul de heliu, interacţionează cu mulţi atomi pe o distanţă foarte mică. Dau naştere la ioni şi îşi consumă toată energia pe acea distanţă scurtă. Cele mai multe particule alfa îşi vor consuma întreaga energie la traversarea unei simple foi de hârtie. Principalul efect asupra sănătatii corelat cu particulele alfa apare când materialele alfa-emiţătoare sunt ingerate sau inhalate, iar energia particulelor alfa afectează ţesuturile interne, cum ar fi plămânii.
- Radiaţia beta (β) sunt compuse din electroni – particule uşoare cu sarcină negativă. Acestea se deplasează pe o distanţă puţin mai mare în aer şi pot trece prin hârtie, dar nu pot penetra prin piele în organismul uman. Efectele asupra sănătăţii asociate particulelor beta se manifestă în principal atunci când materialele beta-emiţătoare sunt ingerate sau inhalate.
- Radiaţia gama (γ) se prezintă sub formă de unde electromagnetice sau fotoni emişi din nucleul unui atom. Ei pot traversa complet corpul uman, putând fi oprite doar de un perete de beton sau de o placă de plumb groasă de 15 cm. Radiaţia gama este oprită de: apă, beton şi, în special, de materiale dense, precum plumbul, folosit ca protectie impotriva expunerii la acest tip de radiaţie. Efectele asupra sănătăţii asociate particulelor gama se manifestă în principal atunci când materialele gama-emiţătoare sunt în afara corpului uman.
- Razele X sunt radiaţii gama cu energie scăzută. În cazul organismului uman, acestea pot penetra ţesuturile musculare, dar nu pot penetra oasele, de unde vine şi utilitatea lor în medicină (radiografii).
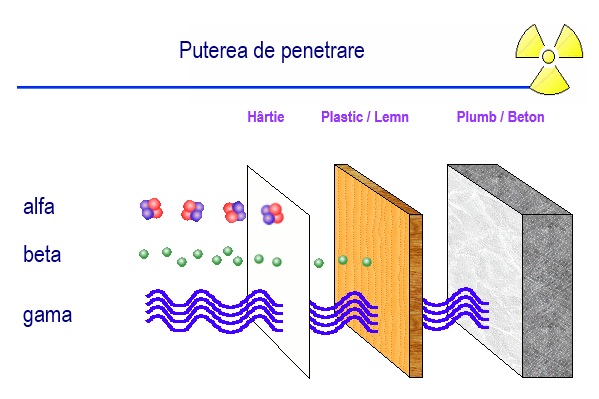
Puterea de penetrare a radiaţiilor ionizante în funcţie de material.
